Gaas ja vedelik
Kõik me oleme kunagi oodanud, et vesi kannus keema läheks. Teame, et temperatuuri tõusuga kaasneb kõigepealt kiirem aurustumine, molekulid hakkavad veepinnalt üha rohkem lahkuma. Muidugi aurustub veidike ka külm vesi – kuna molekulide soojusliikumise kiirused on erinevad, siis leidub alati osakesi, millel on juhuslikult piisavalt liikumisenergiat, et pinnakihist välja pääseda. Vee all, pinnast kaugemal võib samuti olla lahkumiseks piisavalt kiireid molekule. Kui neid on vähe, siis nad välja ei pääse, sest kaotavad aeglasemate molekulidega põrkudes kiiruse.
Aurustumisel pöördub osa molekule pidevalt õhust vette tagasi. Selle tulemusena on veepinna kohal õhk püsivalt niiske, st sisaldab veidi veeauru (ptk Õhuniiskus). Temperatuuri tõusuga saavad vee molekulid hoogu juurde ja hakkavad üha enam veepinnalt lahkuma. Kuid see pole veel keemine. Keemistemperatuuril on kiireid molekule juba nii palju, et intensiivne aurustumine algab kogu vedelikus, mitte ainult pinnal. Tekivad aurumullid, mis kiiresti pinnale tõusevad, vesi on keema läinud. Kuni vett kannus veel on, temperatuur ei tõuse, selles mõttes on keemine sarnane sulamisega (ptk Molekulid. Tahkis).
Mõnikord, kui puhast vett kuumutatakse väga ühtlaselt, ilma segamata (näiteks mikrolaineahjus), võib temperatuur tõusta veidi üle keemistemperatuuri ilma aurumullide tekkimiseta. Kui sellist ülekuumutatud vedelikku veidi liigutada, algab keemine väga äkki. Pliidil ülekuumutatud vett teha ei saa, sest alt soojendamine põhjustab konvektsiooni, segab vett pidevalt ja mullid hakkavad tasapisi tekkima nõu kuumal põhjal.
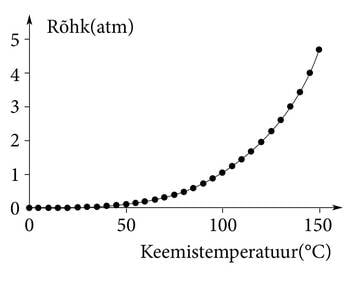
Vee keemistemperatuur valiti juba väga ammu meie igapäevaselt kasutatava praktilise temperatuuriskaala (Celsiuse skaala) üheks aluseks, kindlaks punktiks. Arvatavasti just seepärast teavad kõik, et vesi keeb 100°C juures. Tegelikult sõltub vee keemistemperatuur üsna palju välisrõhust. Keemisel tekivad mullid saavad „ennast täis puhuda” ainult siis, kui aururõhk ületab välisrõhu. Teekannus on väliseks veele mõjuvaks rõhuks õhurõhk. See on küll veidi muutuv, aga igapäevasel teekeetmisel ei pruugi keemistemperatuuri muutuse pärast muretseda.
Mägedes, kus õhurõhk on oluliselt väiksem, tuleb toiduvalmistamisel arvestada, et vesi keeb madalamal temperatuuril. 6000-meetristele mägedele tõustes peavad alpinistid laagris toitu valmistades arvestama umbes 80°C juures keeva veega. Tõsiasja, et puhta vee keemistemperatuur lahtises anumas on otseselt seotud õhurõhuga ning selle kaudu ka päris rahuldavalt kõrgusega merepinnast (ja ka sügavusega allpool merepinda), kasutasid vanasti maadeavastajad ja loodusuurijad kõrguse määramiseks.
Keemistemperatuur. Siiani on jutuks olnud ainult vee keemine. Sobivatel tingimustel keevad ja moodustavad seejuures auru kõik ained, kui nad just kuumutamisel ei lagune. Keemistemperatuur ja selle sõltuvus rõhust on aine olulised füüsikalised omadused. Keemistemperatuuri atmosfäärirõhul on lihtne määrata. Seda muidugi juhul, kui aine üldse atmosfäärirõhul vedelas olekus esineb (ptk Molekulid. Tahkis). Kui vedelik keeb, st aurumullid tekivad ühtlaselt kogu nõus ja termomeeter näitab püsivalt ühte temperatuuri, siis ongi tegemist keemistemperatuuriga. Sulamistemperatuuri määramine on selles mõttes keerulisem, et alati peab kasutama hästi väikest ainekogust (ptk Molekulid. Tahkis).
Segude ja lahuste keemisel on olukord keerulisem. Lahuste keemistemperatuur on kõrgem kui puhtal lahustil. Selle põhjuseks on, et paljud lahustunud ained ei osale aurustumisel, ei lähe üle gaasilisse faasi (aurumullidesse). Lendumatu lahustunud aine aururõhku ei tekita. Keemiseks vajaliku välisrõhuga võrdse aururõhu saavutamiseks tuleb lahust kuumutada veidi kõrgemale temperatuurile. Lahuste keemistemperatuuri erinevus lahustite omast on huvitav nähtus. On selgunud, et keemistemperatuuri muutus sõltub ainult lahustunud osakeste kontsentratsioonist. Ei ole oluline, milline aine on lahustunud ja kas osakesed on ioonid, aatomid või molekulid.
Kas keeta makarone soolases või magedas vees?
Leidub päris palju kokandusnõuandeid, kus soovitatakse kindlasti lisada soola keeduvette, mitte hiljem valmistoidule. Väidetavalt tõstab soola lisamine keemistemperatuuri nii palju, et makaronid keevad kiiremini pehmeks. Jätame maitse-eelistused kõrvale ja küsime, kas keemistemperatuuri tõusust võib oodatud kasu olla?
Lahuste keemistemperatuuri tõus () sõltub lahuse molaalsusest (), lahusti omadusi kirjeldavast ebullioskoopilisest konstandist () ja isotoonilisest kordajast ().
Kui keeduveele lisada ühe liitri kohta 2 teelusikatäit soola (12 g), siis on saadud lahuse molaalsus 0,2 mol/kg. Vee ebullioskoopiline konstant on 0,512 K·kg·mol-1. Isotooniline kordaja kirjeldab aine lahustumisel tekkivate ioonide arvu, keedusoola korral .
Soola lisamisest saadav keemistemperatuuri tõus on tühine, toidu valmimise kiirust see ei mõjuta. Samas on muidugi võimalik, et mingid muud kaalutlused, maitse-eelistused, traditsioonid vms põhjendavad keedusoola koguse ja lisamise aja.
Lahustunud aineks on siin keedusool, mille sulamistemperatuur on 801°C ja keemistemperatuur 1413°C. Kuna vesi ja ka soolvesi keevad palju madalamal temperatuuril, kui keedusool sulab, siis võib öelda, et lahustatud on tahke aine. Täpsemalt, lahustunud aine oleks lahuse keemise temperatuuril tahke. See ei pruugi alati nii olla, näiteks vedelikud võivad lahustuda üksteises ja gaasid võivad lahustuda vedelikes. Isegi tahkes aines võib lahustuda gaas või vedelik.
Vedelikud, gaasid ja aur
Mõned vedelikud segunevad suvalistes vahekordades, näiteks vesi ja etanool. Teised ained moodustavad ühte nõusse valamisel selge piirpinna, näiteks vesi ja bensiin. Täpsemalt uurides selgub siiski, et piirpinnaga eraldatud vedelikud on mõlemad lahused. Bensiini ja vee näites on pealmises kihis bensiin, milles on lahustunud veidi vett ja allpool vesi, milles natuke bensiini. Kui segus on mitu piisavalt erineval temperatuuril keevat vedelikku, võib nende eraldamiseks või puhastamiseks üritada madalaima keemistemperatuuriga aine välja keeta. Seda meetodit nimetatakse destilleerimiseks. Lahustunud gaasid lahkuvad vedelikust muidugi ammu enne keemistemperatuurini jõudmist. Destillatsioon on oluline keemiatööstuse protsess ja just seepärast palju uuritud, teoreetiliselt ja tehnoloogiliselt hästi läbitöötatud. Vaatamata sellele peab ütlema, et vedelike eraldumine keemisel pole kõigis variantides sugugi lihtne nähtus.
Oleme kasutanud segamini mõisteid aur ja gaas. Tegelikult on muidugi iga gaas millegi aur. Näiteks väga madalal temperatuuril ja kõrgel rõhul gaasid veelduvad. Tavatingimustel veeldatud gaasid keevad. Lämmastik on meie atmosfääri põhigaas, teda on õhus kõige rohkem ja me räägime lämmastikust kui gaasist. Samas oleks täiesti korrektne ja teatud juhtudel isegi mõistlik rääkida vedela lämmastiku aurust.
Ained, mida me igapäevaselt nimetame tahketeks (metallid, soolad) sulavad siiski kõrgel temperatuuril, keevad ja aurustuvad. Gaasi ja auru mõisted on tavakeeles seotud sellega, mis olekus ainetega me igapäevaelus ja tehnikas kokku puutume. Näiteks halogeenid lihtainetena: räägime ja kirjutame nagu oleks kloor alati gaas, broom vedelik ja jood kristall. Seepärast on tavatingimustes juttu broomi ja joodi aurudest, aga samas kloorist kui gaasist.
Aine kolm olekut on küll selgelt erinevad, aga neil on paariti mõningaid sarnaseid omadusi. Gaaside ja vedelike ühiseks omaduseks on voolamine ja ainekoguse kindla kuju puudumine, nende ühine nimetus on voolis. Tahkised ja vedelikud on kindla tihedusega olekud, tihedus sõltub temperatuurist ja rõhust suhteliselt vähe. Tahkes ja vedelas olekus lahustuvad ained üksteises enamasti kindlates vahekordades, seepärast saame rääkida küllastunud lahustest, eutektilistest sulamitest ja aseotroopsetest segudest. Tahkiste ja vedelike ühine nimetus on kondensaine. Kuid just gaasiline olek on mõnes mõttes üsna eriline.
Reaalgaasi mudel
Gaasid segunevad kõigis vahekordades. Gaaside tihedus sõltub rõhust ja temperatuurist väga palju, nad on kokkusurutavad ja paisuvad. Ligilähedaselt on gaasi tihedus võrdeline rõhuga ja pöördvõrdeline absoluutse temperatuuriga. Täpselt kehtib see ideaalgaasi korral, aga mitte kõik gaasid ei allu piisavalt hästi ideaalse gaasi mudelile. Meenutame, et ideaalgaasi mudel on rakendatav hõredatele gaasidele (molekulide mõõtmed on võrreldes molekulidevahelise kaugusega tühised), kus molekulid üksteist ei mõjuta (va omavahelised elastsed põrked).
Reaalsed gaasid võivad seega erineda ideaalgaasi mudelist kahel põhjusel:
A) Rõhk. Molekulaarjõud (ptk Van der Waalsi jõud ja vesinikside) mida ideaalgaasi mudelis ei arvestata, sest molekulid on üksteisest kaugel, hakkavad kõrgemal rõhul ja madalamal temperatuuril siiski mõjuma.
Rõhk anuma seinale koosneb mikrotasandil üksikute molekulide elastsetest põrgetest. Ideaalse gaasi molekulid just nii anuma seinale rõhuvadki. Reaalses gaasis on põrke momendil gaasi molekuli ees anuma sein, aga „selja tagant” mõjutavad teda teised gaasi molekulid. Mida tihedamalt molekule ja mida polaarsemad molekulid, seda suurem on mõju.
B) Ruumala. Ideaalgaasi mudel eeldab, et molekulid on punktmassid, st mõõtmeteta. Sel juhul oleks kogu gaasi ruumala gaasi molekulide liikumiseks vaba. Reaalses gaasis võtavad molekulid ise ka ruumi, mida suuremad molekulid ja mida rohkem molekule ruumalaühikus, seda enam.
Reaalseid gaase kirjeldavad ebatavalistes oludes (kondenseerumistemperatuuri lähedal, väga kõrgel rõhul) mitmed reaalgaasi mudelid, kus klassikalisele gaasi olekuvõrrandile lisanduvad vajalikud täiendused.
Milline gaas on kõige ideaalsem? Ideaalse gaasi mudelile vastab kõige täpsemalt gaas, mille molekul on kõige väiksem, ei ole polaarne ja peaaegu ei polariseeru ka ajutiselt. See on heelium, mille molekul koosneb ühest pisikesest aatomist. Ka vesiniku molekul on väike, aga koosneb kahest aatomist, mis võimaldab õige veidi suuremate molekulaarjõudude teket.
Uurime ühte konkreetset reaalgaasi näidet. Millistel tingimustel ja kuivõrd kaldub lämmastik ideaalgaasi mudelist kõrvale?
Meenutame, et ideaalse gaasi olekuvõrrand seob gaasi koguse (), rõhu (), ruumala () ja temperatuuri () gaasi olekuvõrrandisse. R = 8314 J·K-1·kmol-1 (universaalne gaasikonstant).
ja
Saadud jagatis on võrdne ühega, kuni gaas käitub vastavalt ideaalgaasi mudelile. Kui uurida reaalse lämmastiku kokkusurumist või paisumist erinevatel temperatuuridel, siis tuleb välja mitu erinevust.
Joonis 1.2.5. ei ole tegelikult tehtud gaaside ruumala, rõhu ja temperatuuri mõõtmise järgi, vaid kajastab üht enamlevinud reaalgaasi kirjeldust, van der Waalsi võrrandit:
Võrreldes ideaalgaasi lihtsa võrrandiga, võime siin märgata „parandusi”. Konstant kirjeldab molekulide vahelisi mõjusid ja molekulide ruumala.
To summarise
Ideaalgaas
Ideaalgaas on mudel, kus ainsa molekulidevahelise mõjuna arvestatakse elastseid põrkeid ja kus ei arvestata, et lisaks osakestevahelisele tühjusele võtavad ruumi ka molekulid ise.Keemine
Keemine on vedeliku üleminek vedelast faasist gaasilisse, nii et aurustumine ei toimu mitte ainult vedeliku pinnalt, vaid kogu ruumalas tekkivate aurumullidena.
Tahkis ja teised
Tahkiste (tahkete kehade) eripära ilmneb deformeerimisel. Ainult tahkised avaldavad deformeerimisele vastupanu. Vedelike ja tahkiste ühine omadus on säilitada ruumala, mispärast neid nimetatakse kondensaineks.